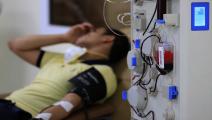
تعد مصر ثاني أكبر دولة أفريقية استضافة للتجارب السريرية
ينص القانون على استطلاع رأي جهاز المخابرات في البحوث
اعترض السيسي على تضمين مشروع القانون حظر تحليل عينات في الخارج
في محاولة لجذب المزيد من التجارب السريرية التي تضمن حصصاً أكبر لمصر من اللقاحات والعلاجات الجديدة لفيروس كورونا، أصدر الرئيس المصري عبد الفتاح السيسي، قبل يومين، قانون تنظيم التجارب الإكلينيكية، بعد تأخر أربعة أشهر تقريباً من موافقة مجلس النواب عليه. وقد استغرقت الرئاسة مدة طويلة لمراجعته، وعرض صياغته النهائية على مختلف الجهات المختصة، وكذلك على عدد من الجهات الدولية، لضمان تأثيره الإيجابي على مجال التجارب السريرية الدوائية الذي كان منتعشاً في مصر قبل فترة جائحة كورونا.
وعلى عكس المنتظر، تعثرت إجراءاته خلال الجائحة، نظراً لعدم ثقة المواطنين في المشاركة بالتجارب، التي أجريت برعاية الحكومة المصرية، ممثلة في وزارة الصحة على اللقاحين الصينيين، اللذين انتهت بالفعل التجارب السريرية على أولهما "سينوفارم" بمشاركة مصرية أقل مما كان منتظراً، ما أثر بالسلب على حصتها الأولية من اللقاحات.
ما زالت مصر لا تستطيع بدء حملتها لحصولها على عدد ضئيل من لقاح كورونا الصيني
وفي الوقت الذي بدأت فيه دول غربية وعربية توزيع اللقاحات في حملات وطنية على الفئات الأولى بالرعاية، ما زالت مصر لا تستطيع بدء حملتها لحصولها على عدد ضئيل من لقاح كورونا الصيني، وعدم توصلها إلى اتفاقات سريعة وكافية حتى الآن، مع المنتجين الأساسيين الحاليين والمتوقعين.
وقال مصدر في وزارة الصحة، لـ"العربي الجديد"، إن مصر لم تستطع تأمين أكثر من نصف عدد المتبرعين للمشاركة في التجارب السريرية على اللقاح، بعد فشل الحملة الدعائية الرسمية بوسائل الإعلام المختلفة والمستشفيات ومراكز التحاليل الحكومية. يأتي ذلك بسبب تخوف المواطنين، الأصحاء والمرضى على حد سواء، من الخضوع للتجارب، على الرغم من أن الأعراض الجانبية الأكثر خطورة التي يمكن أن تترتب على أخذ اللقاح، تقل كثيراً عن أعراض أخرى يمكن أن تترتب على علاجات وأدوية، ينخرط مئات المرضى المصريين سنوياً بموافقتهم، في تجارب سريرية عليها في المستشفيات الحكومية المختلفة.
وأضاف المصدر أن مصر لم تتمكن في الفترة الماضية من اجتذاب فرص المشاركة في عدد من التجارب السريرية، التي تجرى حالياً على لقاحات وعلاجات أخرى لكورونا، بسبب غياب القانون المنظم لتلك الأنشطة، لأن الشركات المختصة كانت أكثر حرصاً على وجود إطار تشريعي منظم للتجارب فيما يخص المستحضرات المرتبطة بالجائحة، أكثر من اهتمامها بنفس الاشتراطات في الأوضاع العادية، ليس فقط بسبب اهتمام الرأي العام العالمي، وانصباب عيون المنظمات الدولية ومعاهد المراقبة الصحية على هذه التجارب. ولكن أيضاً بغية الوصول إلى نتائج دقيقة وسريعة بصورة أكبر من المستحضرات الدوائية العادية، بما في ذلك التي تعالج أو تقي من أمراض ربما تفوق كورونا خطراً، لكنها أقل انتشاراً وليست وبائية.
وتعد مصر وفقاً لتقديرات معاهد الصحة الأميركية والأوروبية ثاني أكبر دولة أفريقية استضافة للتجارب السريرية بعد جنوب أفريقيا، ومن أكثر الدول التي استخدمت لاختبارات الأدوية في الشرق الأوسط، ليس فقط بسبب انخفاض تكلفة البحث، ولكن أيضاً لكثافة أعداد المرضى، من مختلف الأعمار والظروف الصحية، ما يمثل قيمة علمية مضافة، وسهولة منحهم حوافز علاجية ومالية، بسبب افتقار ملايين المصريين لمظلة تأمينية تتيح لهم العلاج بالمجان. ويجعل هذا الأمر المشاركة في تلك التجارب أمراً إيجابياً لشرائح عريضة من المحتاجين، خصوصاً في علاج الأمراض المزمنة والأورام التي يتكلف علاجها بمصر مبالغ مالية باهظة.
وأوضحت المصادر أن هناك تزامناً بين إصدار السيسي للقانون ومطالبة مصر لعدد من شركات الأدوية العالمية، التي لم تطرح لقاحاتها وعلاجاتها بشكل رسمي حتى الآن، للمشاركة في التجارب السريرية الخاصة بها، مقابل الحصول على حصص من تلك المستحضرات. وتحاول القاهرة تلافي تكرار تجربة لقاح "سينوفارم"، إذ أصبح حجم حصة مصر منه رهن المساعدات الإماراتية، والقبول الصيني لعرض القاهرة لافتتاح خط إنتاج له داخل مصر خلال الشهور الستة المقبلة، على أمل توفير حصص إضافية منه للتداول داخل البلاد. وتحاول وزارة الصحة والمخابرات المصريتان حالياً إقناع مسؤولي الشركة والممولين الصينيين لتصبح القاهرة مركزاً لتصنيعه وتوزيعه على مستوى أفريقيا.
وبالنظر إلى النص الذي صدر به القانون الجديد، يتضح أنه ينظم المادة الستين من الدستور، التي تنص على أن "لجسد الإنسان حرمة، والاعتداء عليه، أو تشويهه، أو التمثيل به، جريمة يعاقب عليها القانون. ويحظر الاتجار بأعضائه، ولا يجوز إجراء أية تجربة طبية، أو علمية عليه بغير رضاه الحر الموثق، ووفقاً للأسس المستقرة في مجال العلوم الطبية، على النحو الذي ينظمه القانون". وتعكس طول الفترة بين وضع النص الدستوري وصدور الدستور -والتي تربو على ست سنوات- اختلال أولويات النظام التشريعية.
الشركات المختصة كانت أكثر حرصاً على وجود إطار تشريعي منظم للتجارب فيما يخص المستحضرات المرتبطة بالجائحة
وعلى الرغم من أن القانون بصيغته النهائية يُخفف من العودة للمخابرات العامة ووزارة الدفاع، في العديد من الإجراءات التي كانت تنص عليها صياغته الأولى منذ عامين، فإن الأجهزة، التي توصف في مصر بـ"السيادية"، ستحتفظ بدور كبير بشكل عام في إدارة هذا النشاط العلمي. فالقانون ينص على "استطلاع رأي جهاز المخابرات العامة، في حال البحوث التي تجرى مع جهات أجنبية والدراسات العالمية المشتركة"، بعد الحصول على "موافقة هيئة الدواء المصرية، وموافقة واعتماد المجلس الأعلى، في حال البحوث الطبية الإكلينيكية، التي تشمل استخدام مُركبات دوائية مستحدثة، أو بيولوجية، أو دواعي استعمال جديدة، أو أشكال أو مستلزمات، أو أجهزة طبية لم تستخدم في جسم الإنسان من قبل، ولم تحصل على اعتماد الجهات الدولية، مثل: منظمة الغذاء والدواء الأميركية، أو منظمة الطب الأوروبية، على أن تجرب في دول مرجعية في ذات الوقت".
كما تم تعديل تشكيل المجلس الأعلى لمراجعة أخلاقيات البحوث الطبية الإكلينيكية ليصبح تابعاً لرئيس الوزراء، وسيضم ثلاثة من أعضاء هيئات التدريس في الجامعات، واثنين من الباحثين بالمراكز والمعاهد والهيئات البحثية، وممثلين لوزارة الصحة، وممثل لكل من وزارة الدفاع ووزارة الداخلية والمخابرات العامة ومجلس الدولة، وثلاث شخصيات عامة. وسيكون لهذا المجلس أمانة عامة تتولى القيام بما يكلفها به من مهام، ويرأسها أمين عام يتفرغ لعمله. ويمنح القانون لهيئة الدواء المصرية اختصاصات مهمة، أسوة بهيئة الغذاء والدواء الأميركية، مثل تقييم نتائج البحوث الطبية ما قبل الإكلينيكية وخلالها، والمراجعة العلمية للمستحضر الدوائي أو البيولوجي، وذلك قبل البدء في إجراء البحوث الطبية الإكلينيكية. ويسمح لها بتقييم المخطط البحثي والتعديلات التى ترد عليه، ومراجعة المستندات الخاصة بالمستحضر محل البحث الطبي، وذلك بقصد التأكد من تحقيق الممارسة الطبية الجيدة للتصنيع والتداول والحفظ، والتفتيش على الجهات البحثية التي يجرى بها البحث الطبي الإكلينيكي والجهات ذات الصلة، بغرض التحقق من الممارسة الطبية الجيدة.
وهناك مصطلحان يتضمن القانون شرحاً مقتضباً لهما في التعريفات، لكن لم يتم تفصيلهما بشكل كافٍ في مواده، على الرغم من اعتبارهما من أساسيات نشاط التجارب السريرية العالمية. أولهما الممارسة الطبية الجيدة، والتي عرّفها القانون بأنها مجموعة من المبادئ والمعايير المتعارف عليها دولياً ومحلياً التي تطبق بشأن تخطيط، وإدارة، وتنفيذ، ومراقبة، وتدقيق، وتسجيل، وتحليل، وتقرير البحث الطبي، بقصد توفير الثقة في تمتع البيانات والنتائج المعلنة للبحث بالمصداقية والدقة وصون سلامة المبحوثين المتطوعين وحقوقهم وسرية بياناتهم من أي سوء. وثانيهما الموافقة المستنيرة، والتي عرفها القانون بأنها التعبير المكتوب المبني على إرادة حرة وطواعية كاملة، الذي يصدر عن الشخص ذي الأهلية، ويتضمن موافقته الصريحة توقيعاً، وبصمه على المشاركة في البحث الطبي الإكلينيكي بعد إعلامه وتبصيره بجميع جوانب هذا البحث، وعلى الأخص الآثار أو الأخطار المحتملة التي قد تؤثر على قراره بالمشاركة. وتصدر هذه الموافقة من الممثل القانوني له.
تم تعديل تشكيل المجلس الأعلى لمراجعة أخلاقيات البحوث الطبية الإكلينيكية ليصبح تابعاً لرئيس الوزراء
وذكرت المصادر أنه سيستعان بعدد من القوانين الأجنبية، والاتفاقيات الدولية، لوضع شروط تحقق الممارسات الجيدة والموافقة المستنيرة في اللائحة التنفيذية، التي من المقرر إصدارها خلال ثلاثة أشهر. كما تضمن القانون تعديل جريمة إخراج عينات مصرية للتحليل في الخارج، لتنص المادة العقابية على أن "يعاقب بالحبس وبغرامة لا تقل عن 500 ألف جنيه (نحو 32 ألف دولار أميركي) ولا تزيد على مليون جنيه، أو بإحدى هاتين العقوبتين، كل من ساهم بأي صورة كانت في خروج عينات بشرية تستخدم في الأبحاث الطبية الإكلينيكية أثناء إجرائها، أو بعد انتهائها، دون الحصول مسبقاً على الموافقات المتطلبة وفقاً لأحكام القانون".
وكان السيسي قد اعترض على تضمين مشروع القانون حظر تحليل عينات المصريين في الخارج، وأن ينص القانون على أن إرسال عينات بشرية للخارج يترتب عليه عقوبات سجن وغرامة، حتى لا يتم العبث بالجينات المصرية. وقال، في خطابه للبرلمان، إن الجينات المصرية تمت دراستها بواسطة عدد من الجهات، ومنها مؤسسة أميركية. كما يوجد 10 ملايين مصري في الخارج يمكن بسهولة الحصول على عينات من جيناتهم. وأشار إلى أن هذا النص يتناقض مع تحفيز الجامعات على البحث، وإجراء البحوث المشتركة، كما أن إرسال العينات يتيح الفحص بأجهزة لا تكون متوفرة محلياً.
ومرت محاولات إصدار قانون لتنظيم التجارب السريرية بمراحل غريبة عن السياق المعتاد لإصدار القوانين في عهد السيسي، والتي في الغالب لا تطول مناقشاتها، ولا تبدو بشأنها خلافات واسعة بين أجهزة الحكم. وكانت الحكومة قد وضعت مشروع قانون في العام 2017، ونوقش وأُقر منتصف 2018، وسط اعتراضات علمية واسعة، ليرفض السيسي إقراره في أكتوبر/تشرين الأول من العام نفسه. ثم تراخت الحكومة ومجلس النواب في علاج المشاكل وإقرار المشروع منذ ذلك الوقت، حتى نهاية أغسطس/آب الماضي، عندما وافقت على مشروع معدل يتضمن الاستجابة لملاحظات السيسي، في عجالة لا تعكس طول فترة الانتظار التي طرأت خلالها الجائحة، وزادت في ظلها حاجة المجتمع لضمانات تشريعية للتجارب السريرية.
وكان الاعتراض الأساسي على المشروع في الدوائر العلمية على خلطه بين الأبحاث العلمية والطبية التي تتم لمصلحة جامعات، أو معاهد، في مصر والخارج، والتي تهدف للتعرف على أسباب الأمراض ونتائج العقاقير، وبين التجارب الدوائية التي تتم لحساب شركات أدوية شهيرة، خارج مصر بالأساس، والتي تهدف للتأكد من مطابقة النتائج المترتبة على العقار للدراسات النظرية والتجارب السابق إجراؤها في مناطق أخرى من العالم، تمهيداً لاعتماده والسماح بتداوله. أما السيسي فكانت له مآخذ أخرى على المشروع، مثل المواد التي تتضمن نصوصاً تشترط موافقة المجلس الأعلى للجامعات والمخابرات العامة والهيئات الرقابية على بروتوكول البحث والتفتيش عليه. ونظراً لأن الأبحاث الطبية تشمل رسائل الماجستير والدكتوراه والحرة والممولة في كليات الطب البشري والعلوم والصيدلة، فإن هذا يعني وجود أعداد هائلة كل شهر يستحيل معها متابعة جميع الأبحاث. كما اعترض على انخفاض عدد ممثلي الجامعات المصرية والمعاهد في المجلس الأعلى للبحوث الطبية، المتمثل في أربعة فقط من أصل 15، مع العلم أن 97 في المائة من الأبحاث العلمية تجرى في الجامعات والمعاهد التابعة للتعليم العالي. واعترض أيضاً على أن يتولى الأمانة العامة للمجلس الأعلى رئيس الإدارة المركزية للعلوم الطبية في وزارة الصحة، مع العلم أن الوزارة لا تمثل إلا جزءا ضئيلاً جداً من مجمل هذه الأبحاث في مصر. واعترض السيسي كذلك على أن تكون المواد العقابية من المادة 28 إلى المادة 35 مشددة، ولا تأخذ في عين الاعتبار طبيعة البحث العلمي، وتعتبر المخالفات متساوية بغض النظر عن طبيعة وتصميم البحث، ما يحدث خوفاً شديداً لدى الباحثين، ويتسبب في إعراضهم عن البحث العلمي.